I markedsføringsforordningen er der fastsat krav om, hvilke oplysninger om indhold af fodertilsætningsstoffer i fodermidler og foderblandinger, som det er obligatorisk at angive i mærkningen, hvornår en angivelse er obligatorisk, tolerancer for deklarationen af mængden af tilsætningsstoffer og mulighederne for frivillig mærkning af et indhold af fodertilsætningsstoffer.
28.1 Mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger
Efter markedsføringsforordningen skal indholdet af fodertilsætningsstoffer i fodermidler og foderblandinger angives under overskriften ”Tilsætningsstoffer”.
Reglerne for mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger omfatter:
- obligatorisk mærkning
Her er forskellige mærkningsmuligheder, fordi mængden af de indgående tilsætningsstoffer kan angives på forskellig måder, afhængig af hvad det er for et tilsætningsstof, der mærkes.
- frivillig mærkning
- mærkningsoplysninger, som skal gives, når køberen anmoder den mærkningsansvarlige herom
I markedsføringsforordningen er defineret forkortede navne for en række funktionelle grupper, som fodertilsætningsstoffer indplaceres i.
Markedsføringsforordningen tillader disse forkortede navne. Numrene henviser til de funktionelle gruppers numre i fodertilsætningsstofforordningen.
1h Radionukleidkontrolstoffer
1m Mykotoksinreducerende stoffer
1n Hygiejneforbedrende stoffer
2b Aromastoffer
3a Vitaminer
3b Sporstoffer
3c Aminosyrer
3d Urinstof
4c Miljøforbedrende stoffer
De forkortede navne fremgår af markedsføringsforordningens bilag VI med mærkningsregler for foder til dyr, der anvendes i fødevareproduktionen. Imidlertid er der i bilag VII med mærkningsregler for foder til dyr, der ikke anvendes i fødevareproduktionen, henvist til disse forkortelser, og det betyder, at forkortelserne må bruges i mærkningen af fodertilsætningsstoffer i fodermidler og foderblandinger til alle dyrearter. Disse forkortede navne må bruges, medmindre forkortede navne for funktionelle grupper skulle blive angivet i fodertilsætningsstofforordningen. I så fald skal denne forordnings navne bruges.
Regler brugt i dette afsnit:
Markedsføringsforordningen, artikel 15, litra f), bilag IV og bilag VII, kapitel I og kapitel I, pkt. 3
Fodertilsætningsstofforordningen, bilag I
Se mere i afsnit:
17.1 Betegnelser for dyr
28.2 Fodertilsætningsstoffer der er omfattet af obligatorisk mærkning
Det er obligatorisk at angive indholdet af fodertilsætningsstoffer i fodermidler og foderblandinger:
- når der er fastsat en maksimumgrænse for indholdet af stoffet i foder til mindst én dyreart eller -kategori, der anvendes i fødevareproduktionen.
- når der er fastsat maksimumgrænse for indholdet i foder til mindst én dyreart eller -kategori, der ikke anvendes i fødevareproduktionen.
- for fodertilsætningsstoffer i kategorierne ”zootekniske tilsætningsstoffer” og ”coccidiostatika og histomonostatika”
- for fodertilsætningsstoffer, hvor der er fastsat et anbefalet maksimumindhold, og hvor dette indhold er overskredet. Denne regel er relevant for aromastoffer.
- når indholdet af et fodertilsætningsstof er fremhævet i mærkningen med tekst, med billede eller grafisk.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI, kapitel I, pkt. 1, litra a), og bilag VII, kapitel I, pkt. 1, litra a)-c), og pkt. 4
28.3 Hovedregel for hvad den obligatoriske mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger omfatter
Efter hovedreglen i markedsføringsforordningen skal der i den obligatoriske mærkning gives følgende oplysninger om indholdet af fodertilsætningsstoffer i fodermidler og foderblandinger.
Her skal mængden af tilsætningsstoffet angives som den tilsatte mængde af stoffet.
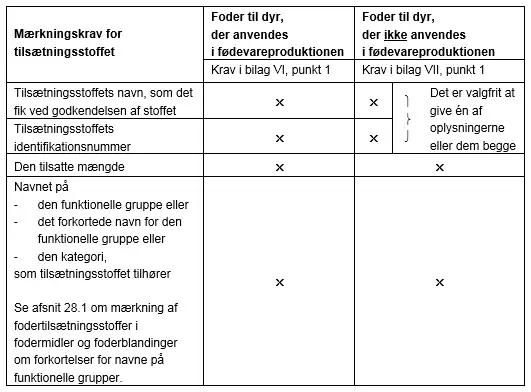
Mærkningsoplysningerne skal gives i overensstemmelse med reglerne i den forordning, hvor fodertilsætningsstoffet er godkendt.
Hvis tilsætningsstoffet tilhører flere funktionelle grupper, skal angives den funktionelle gruppe eller den kategori, som svarer til tilsætningsstoffets hovedfunktion i foderet.
Efter markedsføringsforordningen skal oplysninger om den korrekte anvendelse af fodertilsætningsstoffer i fodermidler og foderblandinger gives i mærkningen, når der er oplysninger herom i godkendelsesforordningen for fodertilsætningsstoffet.
Eksempel på godkendelse af et fodertilsætningsstof – fra forordning 2013/651:
Her er vist, hvor mærkningsoplysningerne kan findes i godkendelsesforordningen.
|
Eksempel
%20.png?width=768)
Godkendelse af fodertilsætningstoffet "Clinoptiolit af sedimentær oprindelse", godkendt i forordningen 2013/651.
|
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI, kapitel 1, pkt. 8 og 9, og VII, kapitel 1, pkt. 1, første- og næstsidste afsnit, pkt. 9 og 10
28.4 Undtagelse for obligatorisk angivelse af mængden af det aktive stof i fodertilsætningsstoffet i fodermidler og foderblandinger
I markedsføringsforordningen er der en undtagelse fra hovedreglen om, at den tilsatte mængde af et fodertilsætningsstof skal angives i mærkningen, når der er angivet et stof i kolonnen ”Minimumsindhold/Maksimumsindhold” i godkendelsen af et fodertilsætningsstof. I disse tilfælde er det obligatorisk at angive den tilsatte mængde af dette stof i stedet for den tilsatte mængde af fodertilsætningsstoffet
|
Eksempler på stoffer, der skal mærkes efter denne undtagelse
|
|
I kolonnen ”Minimumsindhold/Maksimumsindhold” kan være nævnt:
|
Typer af fodertilsætningsstoffer:
|
|
-mg aktivstof/kg
|
Når det er defineret hvad aktivstoffet er
|
|
-internationale enheder (IU)/kg
|
Nogle vitaminer
|
|
-mg ad grundstoffet/kg
|
Sporstoffer
|
|
-enzymaktivitetsenheder/kg
|
Fodertilsætningsstoffer, der er enzymer
|
|
-antallet af kolonier af mikroorganismer/kg
|
Fodertilsætningsstoffer, der er mikroorganismer
|
Eksempel på godkendelse af et fodertilsætningsstof, hvor det aktive stof i fodertilsætningsstoffet er angivet i kolonnen ”Minimumsindhold/Maksimumsindhold” – kun et uddrag af teksten fra forordning 2016/1095:
I eksemplet er vist, hvor mærkningsoplysningerne kan findes i godkendelsesforordingen.
|
Eksempel på mærkningskrav, når det aktive stof i fodertilsætningsstoffet er angivet i kolonnen "Miniumindhold/Maksimumsindhold"

Godkendelse af fodertilsætningsstoffet zinkacetat-dihydrat, godkendt i forordningen 2016/1095.
|
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI og VII, kapitel I, pkt. 1, sidste afsnit
28.5 Obligatorisk mærkning når det totale indhold angives under Analytiske bestanddele
Den tilsatte mængde af et fodertilsætningsstof skal ii udgangspunktet angives i mærkningen. Hvis der i godkendelsen af et fodertilsætningsstof, er angivet et stof i kolonnen ”Minimumsindhold/Maksimumsindhold”, skal den tilsatte mængde af det pågældende aktive stof dog angives i mærkningen i stedet for mængden af tilsætningsstoffet.
I stedet for angivelse af mængden af fodertilsætningsstoffer efter ovenstående to muligheder, tillades også som alternativ, at mængden af vitaminer, provitaminer og kemisk veldefinerede stoffer med tilsvarende virkning angives som det totale indhold af stoffet, dvs. summen af det naturlige og det tilsatte indhold. Totalindholdet skal angives under ”Analytiske bestanddele” i stedet for den tilsatte mængde under ”Tilsætningsstoffer”. Med denne mærkningsmulighed kan der bl.a. tages højde for tab af vitaminer under produktionsprocessen.
Forudsætningen for denne mærkning er:
- Den samlede mængde af vitaminet skal angives, dvs. summen af det naturlige og det tilsatte indhold.
- Det samlede indhold, garanteret i hele holdbarhedsperioden, skal angives.
- Vitaminindholdet skal angives under overskriften ”Analytiske bestanddele” og ikke angives under overskriften ”Tilsætningsstoffer”.
Øvrige oplysninger, som skal gives om de indgående fodertilsætningsstoffer, skal angives efter hovedreglen.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI og VII, kapitel I, pkt. 2
Se mere i afsnit:
22.10 Angivelse af indholdet af analytiske bestanddele i foderblandinger
28.6 Tolerancer for deklaration af fodertilsætningsstoffer i foderblandinger og fodermidler
I forbindelse med deklarationen af et indhold af et fodertilsætningsstof under overskriften ”tilsætningsstoffer” eller ”analytiske bestanddele” gælder følgende tolerancer for et konstateret indhold under det deklarerede indhold:
- 10 % af det angivne indhold, hvis det angivne indhold er 1 000 enheder eller derover
- 100 enheder, hvis det angivne indhold er under 1 000 enheder, men ikke under 500 enheder
- 20 % af det angivne indhold, hvis det angivne indhold er under 500 enheder, men ikke under 1 enhed
- 0,2 enheder, hvis det angivne indhold er under 1 enhed, men ikke under 0,5 enhed
- 40 % af det angivne indhold, hvis det angivne indhold er under 0,5 enhed.
Dog gælder der ingen tolerance ud over et minimumsindhold fastsat i godkendelsen af stoffet.
For et konstateret indhold over det deklarerede accepteres en tolerance på op til 3 gange de angivne tolerancer ovenfor (a-e), dog gælder der ingen tolerance udover et maksimumsindhold fastsat i godkendelsen af stoffet.
Tolerancerne er fastsat enten som en absolut værdi f.eks. 100 enheder eller som en relativ værdi f.eks. 20 % af det angivne indhold afhængig af størrelsen af den deklarerede værdi.
Det er de samme tolerancer, der gælder for deklaration af den tilsatte mængde under ”tilsætningsstoffer” som for deklaration af det totale indhold (naturligt + tilsat indhold) under ”analytiske bestanddele”.
I enkelte tilfælde, hvor det er et krav, at indholdet af et fodertilsætningsstof angives som den tilsatte mængde angives under overskriften ”tilsætningsstoffer”, kan et samtidigt naturligt højt indhold af samme stof fra et eller flere af de anvendte fodermidler medføre, at den deklarerede mængde ikke overholder de ovenfor angivne tolerancer. Er der f.eks. tale om stoffer omfattet af den funktionelle gruppe ”vitaminer, provitaminer og kemiske veldefinerede stoffer med tilsvarende virkning”, kan det derfor være hensigtsmæssigt, at deklarere det totale indhold under overskriften ”analytiske bestanddele” i stedet for den tilsatte mængde under ”tilsætningsstoffer”.
I tilfælde, hvor det ikke er tilladt at erstatte deklarationen af den tilsatte mængde under ”tilsætningsstoffer” med en deklaration af det totale indhold under ”analytiske bestanddele” er det Fødevarestyrelsens vurdering, at det i helt særlige tilfælde ikke altid er muligt at deklarere indholdet i overensstemmelse med tolerancerne, såfremt der er et højt naturligt indhold af samme stof i et eller flere af de anvendte fodermidler. I sådanne særlige tilfælde er det Fødevarestyrelsens praksis, at der ikke sanktioneres for et overindhold af det deklarerede fodertilsætningsstof.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag IV, del B
28.7 Frivillig mærkning af sensoriske fodertilsætningsstoffer eller tilsætningsstoffer med ernæringsmæssige egenskaber, når disse ikke er omfattet af obligatorisk mærkning
Når et sensorisk tilsætningsstof eller et tilsætningsstof med ernæringsmæssige egenskaber ikke er omfattet af kravet om obligatorisk mærkning, men angives ved frivillig mærkning, skal tilsætningsstoffet mærkes efter mærkningsreglerne for obligatorisk mærkning.
Fodertilsætningsstoffet skal angives i mærkningen:
- enten som den obligatoriske angivelse af den tilsatte mængde af fodertilsætningsstoffet,
- eller som den obligatoriske angivelse af mængden af det aktive stof i fodertilsætningsstoffet.
Derudover er der et frivilligt alternativ for vitaminer, provitaminer og kemisk veldefinerede stoffer:
- Mærkning af totalindholdet af stoffet under overskriften ”Analytiske bestanddele” i stedet for angivelse under ”Tilsætningsstoffer”. Alle øvrige oplysninger om indholdet end angivelsen af mængden af vitaminet skal ske efter hovedreglen.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI, kapitel I, pkt.7, og bilag VII, kapitel I, pkt. 8
Se mere i afsnit:
28.3 Hovedregel for hvad den obligatoriske mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger omfatter
28.4 Undtagelse for obligatorisk angivelse af mængden af det aktive stof i fodertilsætningsstoffet i fodermidler og foderblandinger
28.5 Obligatorisk mærkning når det totale indhold angives under Analytiske bestanddele
28.8 Frivillig mærkning af ”andre” fodertilsætningsstoffer i fodermidler og foderblandinger
For fodertilsætningsstoffer,
- som det ikke er obligatorisk at angive i mærkningen,
- og som hverken er sensoriske fodertilsætningsstoffer eller tilsætningsstoffer med ernæringsmæssige egenskaber
er det tilladt frivilligt at angive disse ”andre” fodertilsætningsstoffer i mærkningen.
Følgende mærkning skal angives for disse ”andre” fodertilsætningsstoffer:
- Indholdet skal som minimum angives med fodertilsætningsstoffets navn.
For aromastoffer skal indholdet som minimum angives ved deres funktionelle gruppe.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI, kapitel I, pkt. 6, og bilag VII, kapitel I, pkt. 7
28.9 Tilladt mærkning af sensoriske tilsætningsstoffer eller tilsætningsstoffer med ernæringsmæssige egenskaber
Markedsføringsforordningen tillader, at det totale indhold – summen af det naturlige indhold og det tilsatte indhold af følgende fodertilsætningsstoffer – angives under overskriften ”Analytiske bestanddele”.
- Tilsætningsstoffer med ernæringsmæssige egenskaber, dvs. fodertilsætningsstoffer som tilhører de funktionelle grupper (forkortede navne) ”vitaminer”, ”sporstoffer”, ”aminosyrer” eller ”urinstof”, eller
- Sensoriske tilsætningsstoffer.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI, kapitel I, pkt. 7, og kapitel II, pkt. 2, samt bilag VII, kapitel I, pkt.8, og kapitel II, pkt. 2
Se mere i afsnit:
22.10 Angivelses af indholdet af analytiske bestanddele i foderblandinger
28.10 Undtagelse for mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger til dyr, der ikke anvendes i fødevareproduktionen
Ved mærkning af indholdet af fodertilsætningsstoffer i fodermidler og foderblandinger til dyr, der ikke anvendes i fødevareproduktionen, kan man nøjes med at mærke foderet med navnet på den funktionelle gruppe for disse fodertilsætningsstoffer:
- ”konserveringsmidler”,
- ”antioxidanter”,
- ”farvestoffer” og
- ”aromastoffer”
Når indholdet af fodertilsætningsstoffer er mærket efter undtagelsen, og køberen anmoder om at få oplysning om foderets sammensætning, skal den mærkningsansvarlige give køberen de oplysninger om tilsætningsstofferne, som skal gives efter den obligatoriske mærkning:
- Enten oplysning om den tilsatte mængde af fodertilsætningsstoffet,
- eller oplysning om den tilsatte mængde af det aktive stof i fodertilsætningsstoffet.
Købere af foder til selskabsdyr kan anmode om at få oplysninger om fodertilsætningsstofferne, der indgår i fodermidlet eller foderblandingen, ved hjælp af det frikaldsnummer, som foder til selskabsdyr skal være mærket med.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VII, kapitel I, pkt.5
Se mere i afsnit:
24.1 Mærkning af foder til selskabsdyr – supplement til mærkningen af fodermidler, foderblandinger eller diætetisk
28.3 Hovedregel for hvad den obligatoriske mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger omfatter
28.4 Undtagelse for obligatorisk angivelse af mængden af det aktive stof i fodertilsætningsstoffet i fodermidler og foderblandinger
28.11 Oplysning om indhold af fodertilsætningsstoffer, der skal gives, når køber anmoder herom
I de tilfælde, hvor det ikke er obligatorisk at angive indholdet af fodertilsætningsstoffer i mærkningen af et fodermiddel eller en foderblanding, kan køberen anmode om at få oplyst indholdet af disse fodertilsætningsstoffer.
Den mærkningsansvarlige skal oplyse tilsætningsstoffets:
- navn,
- identifikationsnummer og
- den funktionelle gruppe.
Denne bestemmelse gælder ikke for aromastoffer.
Regler brugt i dette afsnit:
Markedsføringsforordningen, bilag VI, kapitel I, pkt. 5 og bilag VII, kapitel I, pkt. 6
Se mere i afsnit:
28.2 Fodertilsætningsstoffer der er omfattet af obligatorisk mærkning
28.3 Hovedregel for hvad den obligatoriske mærkning af fodertilsætningsstoffer i fodermidler og foderblandinger omfatter
28.4 Undtagelse for obligatorisk angivelse af mængden af det aktive stof i fodertilsætningsstoffet i fodermidler og foderblandinger
28.5 Obligatorisk mærkning når det totale indhold angives under Analytiske bestanddele
28.12 Mærkning af foderlægemidler og mellemprodukter
De specifikke krav til mærkning af foderlægemidler og mellemprodukter skal overholde bilag III i foderlægemiddelforordningen
Foderlægemiddelforordningens artikel 9
Desuden finder de særlige krav, der er fastsat i markedsføringsforordningen (EF) nr. 767/2009) for mærkning af fodermidler og foderblandinger, anvendelse på foderlægemidler og mellemprodukter.
Markedsføringsforordningens artikel 16 og 17
Anvendes der beholdere i stedet for pakninger, for eksempel hvis foderlægemidler leveres i bulk, skal disse ledsages af et dokument, som overholder reglerne beskrevet ovenfor.
Se mere om de særlige mærkningskrav for fodermidler og foderblandinger i
Afsnit 22.4 Mærkning af fodermidler - supplement til ”Basismærkningen”
Afsnit 22.7 Mærkning af foderblandinger - supplement til ”Basismærkningen”
Tolerancer
De tilladte tolerancer for afvigelser mellem det på mærkningen angivne indhold af et virksomt stof i et foderlægemiddel eller et mellemprodukt og det indhold, der måles ved analyser som led i den offentlige kontrol i henhold til kontrolforordningen (EU) 2017/625, skal være som følger:
| Virksomt stof pr. kg foderlægemiddel eller mellemprodukter |
Tolerancer |
| > 500 mg |
± 10 % |
| ≤ 500 mg |
± 20 % |
Det betyder, at hvis man som virksomhed eksempelvis producerer et foderlægemiddel, der indeholder 600 mg (dvs. > 500 mg) virksomt stof pr. kg foderlægemiddel/mellemprodukt, så er det tilladte interval for analytisk målt indhold af det virksomme stof, i forbindelse med den offentlige kontrol, på 440 mg til 560 mg (± 10 %) virksomt stof pr. kg foderlægemiddel/mellemprodukt.
Foderlægemiddelforordningens bilag IV
Reklame
Reklame for foderlægemidler og mellemprodukter er forbudt, undtagen reklame der udelukkende er henvendt til dyrlæger.
Foderlægemiddelforordningen, artikel 11
Reklame henvendt til dyrlæger må ikke lede til en forkert anvendelse af foderlægemidlet. Foderlægemidler må ikke uddeles i reklameøjemed, undtagen som prøver i små mængder. Disse prøver skal være mærket med angivelse af, at det er prøver, som skal gives direkte til dyrlæger.
Foderlægemidler, der indeholder antimikrobielle veterinærlægemidler, må ikke uddeles som prøver.
Regler brugt i dette afsnit:
Foderlægemiddelforordningen, artikel 9, artikel 11 og bilag IV
Markedsføringsforordningen, artikel 16 og artikel 17